ASPERGILOSIS PULMONAR INVASIVA
El Aspergillus es un hongo que se encuentra ampliamente distribuido por todo el mundo. Entre sus numerosas especies, el Aspergillus fumigatus es el causante de, aproximadamente, 90% de las infecciones en humanos. El pulmón es el principal órgano afectado por el Aspergillus debido a la alta capacidad esporulativa de este hongo, y a que sus conidias son lo suficientemente pequeñas para poder alcanzar el alveolo1.
El Aspergillus spp puede causar varias enfermedades como son el aspergiloma, la aspergilosis broncopulmonar alérgica o la aspergilosis pulmonar invasiva (API)2.
La API en pacientes con enfermedad pulmonar obstructiva crónica (EPOC) es una enfermedad grave, con una tasa de mortalidad elevada, entre 91% y 95%2,3. Parecen un factor relevante para este mal pronóstico las dificultades diagnósticas, derivadas de la inespecificidad de la presentación clínica y de la ausencia de pruebas complementarias no invasivas que puedan considerarse definitivas2,4. Además, en pacientes sin datos de inmunodepresión conocida, el diagnóstico puede retrasarse más por no plantearse inicialmente la posibilidad diagnóstica de API5.
A lo largo de las pasadas dos décadas se ha producido un incremento significativo de la incidencia de API, especialmente en pacientes gravemente inmunodeprimidos, como los tratados con quimioterapia o trasplantados. Pero en los últimos años también se ha visto, cada vez con más frecuencia, asociada a otras enfermedades, entre las cuales se incluye la EPOC2,3,6. Actualmente, entre 30% y 50% de casos de API se diagnostican en pacientes no neutropénicos, con una mortalidad similar a los neutropénicos4,7.
Este incremento de incidencia hace que, para algunos autores, la EPOC deba incluirse entre las patologías de base con alto riesgo de API8. La mayoría, aunque no todos, de los pacientes con EPOC que desarrollan API estaban en tratamiento con corticoides sistémicos2,3,8,9. Bulpa et al, en una revisión de varias series, encuentran que 43 de los 56 pacientes estudiados habían recibido corticoi-des en el momento del ingreso y, de éstos, 3 los habían tomado únicamente de forma inhalada2.
La falta de una definición consensuada, la ausencia de medidas de vigilancia de la infección, o la dificultad para diferenciar la colonización de la infección hacen que la incidencia de la API asociada a la EPOC sea difícil de valorar2.
Actualmente, el diagnóstico de API, tanto en la categoría de probada, probable o posible, está realizada en base a una población de pacientes inmunodeprimidos, fundamentalmente oncológicos y trasplantados, altamente susceptible a las infecciones fúngicas10,11. Recientemente se han propuesto los criterios de API posible, probable y probada en pacientes con EPOC (Tabla 1)2.
El Aspergillus spp puede causar varias enfermedades como son el aspergiloma, la aspergilosis broncopulmonar alérgica o la aspergilosis pulmonar invasiva (API)2.
La API en pacientes con enfermedad pulmonar obstructiva crónica (EPOC) es una enfermedad grave, con una tasa de mortalidad elevada, entre 91% y 95%2,3. Parecen un factor relevante para este mal pronóstico las dificultades diagnósticas, derivadas de la inespecificidad de la presentación clínica y de la ausencia de pruebas complementarias no invasivas que puedan considerarse definitivas2,4. Además, en pacientes sin datos de inmunodepresión conocida, el diagnóstico puede retrasarse más por no plantearse inicialmente la posibilidad diagnóstica de API5.
A lo largo de las pasadas dos décadas se ha producido un incremento significativo de la incidencia de API, especialmente en pacientes gravemente inmunodeprimidos, como los tratados con quimioterapia o trasplantados. Pero en los últimos años también se ha visto, cada vez con más frecuencia, asociada a otras enfermedades, entre las cuales se incluye la EPOC2,3,6. Actualmente, entre 30% y 50% de casos de API se diagnostican en pacientes no neutropénicos, con una mortalidad similar a los neutropénicos4,7.
Este incremento de incidencia hace que, para algunos autores, la EPOC deba incluirse entre las patologías de base con alto riesgo de API8. La mayoría, aunque no todos, de los pacientes con EPOC que desarrollan API estaban en tratamiento con corticoides sistémicos2,3,8,9. Bulpa et al, en una revisión de varias series, encuentran que 43 de los 56 pacientes estudiados habían recibido corticoi-des en el momento del ingreso y, de éstos, 3 los habían tomado únicamente de forma inhalada2.
La falta de una definición consensuada, la ausencia de medidas de vigilancia de la infección, o la dificultad para diferenciar la colonización de la infección hacen que la incidencia de la API asociada a la EPOC sea difícil de valorar2.
Actualmente, el diagnóstico de API, tanto en la categoría de probada, probable o posible, está realizada en base a una población de pacientes inmunodeprimidos, fundamentalmente oncológicos y trasplantados, altamente susceptible a las infecciones fúngicas10,11. Recientemente se han propuesto los criterios de API posible, probable y probada en pacientes con EPOC (Tabla 1)2.
Fisiopatología
Las diferentes formas clínicas derivadas de la presencia de Aspergillus spp en la vía aérea deben verse como un proceso evolutivo, que se inicia en la colonización de la vía aérea, continúa con la ruptura de la barrera epitelial por las hifas del hongo (evento inicial de la invasión tisular), progresando a API, pudiendo posteriormente diseminarse al resto del organismo7.
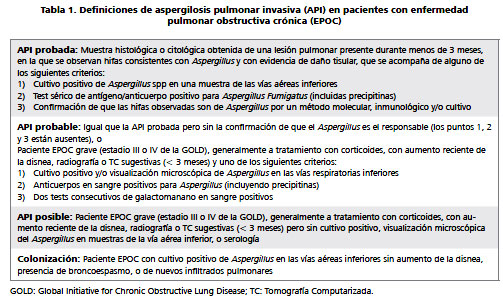
No se conoce de forma definitiva el motivo por el cual algunos pacientes con EPOC desarrollan API, pero se han descrito diversos factores que parecen favorecer esta evolución (Tabla 2). El daño pulmonar será distinto según el estado inmuno-lógico de los pacientes. En los neutropénicos se produce angioinvasión, hemorragia intraalveolar, e infartos pulmonares (Figura 1). En los no neu-tropénicos se producirá necrosis inflamatoria, pero sin invasión vascular, hemorragia o infarto12. Este modelo de lesión pulmonar no angioinvasiva también es el aspecto más característico de la API en modelos animales sometidos a tratamiento corticoideo12.
Las diferentes formas clínicas derivadas de la presencia de Aspergillus spp en la vía aérea deben verse como un proceso evolutivo, que se inicia en la colonización de la vía aérea, continúa con la ruptura de la barrera epitelial por las hifas del hongo (evento inicial de la invasión tisular), progresando a API, pudiendo posteriormente diseminarse al resto del organismo7.
No se conoce de forma definitiva el motivo por el cual algunos pacientes con EPOC desarrollan API, pero se han descrito diversos factores que parecen favorecer esta evolución (Tabla 2). El daño pulmonar será distinto según el estado inmuno-lógico de los pacientes. En los neutropénicos se produce angioinvasión, hemorragia intraalveolar, e infartos pulmonares (Figura 1). En los no neu-tropénicos se producirá necrosis inflamatoria, pero sin invasión vascular, hemorragia o infarto12. Este modelo de lesión pulmonar no angioinvasiva también es el aspecto más característico de la API en modelos animales sometidos a tratamiento corticoideo12.
CUADRO CLINICO
En un paciente con EPOC, con un cuadro clínico sugestivo de infección respiratoria, e infiltrados pulmonares, que no responde al tratamiento antibiótico de amplio espectro, debe contemplarse la posibilidad de API2,3,9.
Predomina en varones con una edad media de 65 años. El tratamiento corticoideo sistémico está presente en 70% de los casos ya antes del ingreso, y alcanza a 87% de los pacientes durante el ingreso hospitalario2.
Los síntomas de presentación son muy variables. Lo más frecuente es la disnea (32%-48% de casos), febre (39%), tos (26%), sibilancias (8%-28%) o hemoptisis (12%-15%). Otros síntomas son menos frecuentes, como el incremento de expectoración o el dolor torácico2,3.
Con cierta frecuencia no suele sospecharse la aspergilosis, contemplándose otras posibilidades diagnósticas. Las hipótesis diagnósticas más frecuentemente establecidas al diagnóstico son la insuficiencia respiratoria aguda (41% de los casos), EPOC agudizado (34%), neumonía (20%), e incluso shock séptico en un 5% de pacientes3.
El retraso entre el inicio de los síntomas y el diagnóstico (mediana de 8,5 días), puede ser una de las causas de la morbimortalidad de esta enfermedad2.
Los datos de la analítica sanguínea son inespecíficos. Suelen revelar leucocitosis, aumento de la proteína C reactiva, del fibrinógeno y de la lactato deshidrogenasa (LDH). También pueden presentar trombocitopenia leve2.
Exploraciones complementarias en el diagnóstico de la API
Ante la sospecha de infección respiratoria, se realizará cultivo de esputo. Su utilidad es limitada. La sensibilidad está alrededor de 50%. Además puede haber otras especies de hongos, pero cuya respuesta al tratamiento es distinta2,3. Esta sensibilidad puede aumentar hasta 88% si se utilizan técnicas de fluorescencia29.
Aunque el Aspergillus spp pueda crecer en un medio de cultivo común, el crecimiento es mejor en medio específico para hongos. El cultivo positivo para Aspergillus spp no es diagnóstico per se, pero incrementará la sospecha de infección cuando el paciente no responde a antibióticos y, especialmente, en los pacientes tratados con este-roides. Los cultivos positivos repetidos son más sugestivos de infección30.
El cultivo de las secreciones respiratorias tiene un valor añadido al del diagnóstico clínico, ya que nos permitirá identificar la sensibilidad del germen a los fármacos disponibles31.
Cuando no se dispone de esputo, el material para cultivo se obtendrá por fibrobroncoscopia. La rentabilidad de los cultivos varía entre 46 y 77%32,33, mientras que se demostraron rentabilidades más bajas en pacientes que recibían tratamiento antifúngico34. La utilidad diagnóstica de las muestras obtenidas por broncoscopia es superior en casos de neumonía prolongada o de lesiones pulmonares extensas. Brown et al35 sugieren que la positividad del lavado broncoalveolar (BAL) depende del tipo de API: 20% en la forma angio-invasiva y 80% en la forma invasiva de la vía aérea. Curiosamente, el examen citológico parece ser más a menudo positivo que los cultivos36.
Serología
El antígeno galactomanano (GM) es un marcador de la diseminación hematógena del hongo, muy utilizado en pacientes neutropénicos, donde parece útil para establecer la sospecha de API antes de la aparición de la sintomatología. Su evaluación dos veces por semana permite ver la evolución de los niveles de galactomanano37. La antigenemia positiva precedió a la febre en 3,5 días, a los hallazgos en la radiografía simple de tórax en 8 días, a la TAC torácica en 6 días y a los resultados del primer cultivo de secreciones respiratorias en 9 días37. Para obtener estos resultados, las muestras de sangre deben tomarse al menos 2 veces por semana38. El GM también se puede detectar en el BAL, orina o líquido céfalo raquídeo3.
En pacientes no neutropénicos es más difícil de valorar. No está bien establecido el valor de una determinación puntual; y parece difícil su medición repetida en pacientes no neutropénicos. En pacientes no neutropénicos los resultados son contradictorios. Unos autores defenden su utilidad, con una sensibilidad de 88% y especificidad de 87%39; y por el contrario, otros destacan los falsos positivos relacionados con la colonización fúngica en el lavado broncoalveolar de los pacientes no inmunodeprimidos con infiltrados pulmonares40.
Globalmente el GM tiene una sensibilidad de 71% y una especificidad de 89%, con un valor predictivo positivo entre 25% y 62%, y un valor predictivo negativo entre 92% y 98%, aunque con gran variabilidad entre los diferentes estudios41,42. Estas discrepancias se deben, entre otras causas, al número de tests realizados por semana, la definición utilizada de API y el punto de corte elegido37,41,42.
Una modificación en el proceso de las muestras de suero permite un incremento significativo de la sensibilidad del test de GM, además de acortar los tiempos de diagnóstico, aunque con una discreta disminución en la especificidad43.
El GM también se ha aplicado en pacientes con EPOC gravemente enfermos y sospecha de API. En un estudio con 25 pacientes, 12 fueron positivos (40%). Sin embargo, no se pueden extraer conclusiones definitivas debido a la pequeña muestra, el diseño retrospectivo del estudio y la ausencia de investigación sobre la existencia de factores confusores9. Una única determinación de GM podría ser útil para el diagnóstico de la API en pacientes no hematológicos44.
Un incremento en la antigenemia sobre un valor basal puede discriminar mejor que un simple valor por encima del normal. La elevación de la antigenemia durante la primera semana de observación estaba asociado con enfermedad progresiva, con una sensibilidad de 44%, una especificidad de 87%, y un valor predictivo positivo de 94%44. Un aumento en la antigenemia también podría ser indicativo de fallo en el tratamiento y, por tanto, nos permitiría anticipar la decisión de modificar el tratamiento45.
El test del GM tiene varias limitaciones. Solamente un tercio de los pacientes tenían una respuesta antigénica positiva antes de que el diagnóstico de API se hiciera por TC. Tampoco se ha demostrado reducción de la mortalidad con la utilización de esta prueba. Se han descrito falsos positivos en pacientes que estaban recibiendo tratamiento con piperacilina/tazobactan o amoxicilina/clavulánico; así como reacciones cruzadas con otros hongos, bacterias, ciclofosfamida y comidas (vegetales enlatados, pasta, arroz). Por último, se desconoce si los resultados obtenidos en enfermedades hematológicas malignas pueden extrapolarse a pacientes con otras enfermedades como la EPOC2,7,33,38,46,47.
Otras exploraciones de laboratorio, como la reacción en cadena de la polimerasa (PCR) o la concentración plasmática de β-D-glucano están en desarrollo. Resultados preliminares sugieren que la PCR tiene una buena sensibilidad y especificidad48. Sin embargo, no hay métodos estandarizados y validados, las definiciones de API varían en los distintos estudios y hay que ser precavidos porque productos del plasma podrían inhibir los test de PCR49. La determinación de la concentración plasmática de β-D-glucano, un componente de la pared celular del hongo, no parece superior a los test de PCR50.
Por otra parte, la producción de anticuerpos traduce la respuesta de la inmunidad humoral.
Constituyen un criterio diagnóstico en otras formas de enfermedad por Aspergillus, aunque su papel no está clarificado en la API7.
Radiología
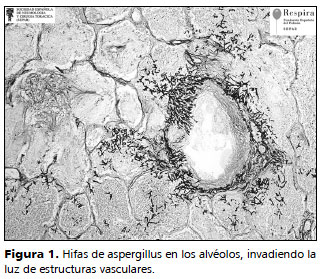
La radiografía de tórax puede ser normal en los estadios iniciales de la API. Se han descrito múltiples signos radiológicos asociados con API, tales como consolidación, nódulos, el signo del halo o el signo del aire creciente. Lo más frecuente es la presentación de consolidación pulmonar, que presentan alrededor de 60% de pacientes3,11.
En un contexto clínico compatible, la presencia de una o varias opacidades nodulares debe hacernos sospechar API (Figura 2).
Predomina en varones con una edad media de 65 años. El tratamiento corticoideo sistémico está presente en 70% de los casos ya antes del ingreso, y alcanza a 87% de los pacientes durante el ingreso hospitalario2.
Los síntomas de presentación son muy variables. Lo más frecuente es la disnea (32%-48% de casos), febre (39%), tos (26%), sibilancias (8%-28%) o hemoptisis (12%-15%). Otros síntomas son menos frecuentes, como el incremento de expectoración o el dolor torácico2,3.
Con cierta frecuencia no suele sospecharse la aspergilosis, contemplándose otras posibilidades diagnósticas. Las hipótesis diagnósticas más frecuentemente establecidas al diagnóstico son la insuficiencia respiratoria aguda (41% de los casos), EPOC agudizado (34%), neumonía (20%), e incluso shock séptico en un 5% de pacientes3.
El retraso entre el inicio de los síntomas y el diagnóstico (mediana de 8,5 días), puede ser una de las causas de la morbimortalidad de esta enfermedad2.
Los datos de la analítica sanguínea son inespecíficos. Suelen revelar leucocitosis, aumento de la proteína C reactiva, del fibrinógeno y de la lactato deshidrogenasa (LDH). También pueden presentar trombocitopenia leve2.
Exploraciones complementarias en el diagnóstico de la API
Ante la sospecha de infección respiratoria, se realizará cultivo de esputo. Su utilidad es limitada. La sensibilidad está alrededor de 50%. Además puede haber otras especies de hongos, pero cuya respuesta al tratamiento es distinta2,3. Esta sensibilidad puede aumentar hasta 88% si se utilizan técnicas de fluorescencia29.
Aunque el Aspergillus spp pueda crecer en un medio de cultivo común, el crecimiento es mejor en medio específico para hongos. El cultivo positivo para Aspergillus spp no es diagnóstico per se, pero incrementará la sospecha de infección cuando el paciente no responde a antibióticos y, especialmente, en los pacientes tratados con este-roides. Los cultivos positivos repetidos son más sugestivos de infección30.
El cultivo de las secreciones respiratorias tiene un valor añadido al del diagnóstico clínico, ya que nos permitirá identificar la sensibilidad del germen a los fármacos disponibles31.
Cuando no se dispone de esputo, el material para cultivo se obtendrá por fibrobroncoscopia. La rentabilidad de los cultivos varía entre 46 y 77%32,33, mientras que se demostraron rentabilidades más bajas en pacientes que recibían tratamiento antifúngico34. La utilidad diagnóstica de las muestras obtenidas por broncoscopia es superior en casos de neumonía prolongada o de lesiones pulmonares extensas. Brown et al35 sugieren que la positividad del lavado broncoalveolar (BAL) depende del tipo de API: 20% en la forma angio-invasiva y 80% en la forma invasiva de la vía aérea. Curiosamente, el examen citológico parece ser más a menudo positivo que los cultivos36.
Serología
El antígeno galactomanano (GM) es un marcador de la diseminación hematógena del hongo, muy utilizado en pacientes neutropénicos, donde parece útil para establecer la sospecha de API antes de la aparición de la sintomatología. Su evaluación dos veces por semana permite ver la evolución de los niveles de galactomanano37. La antigenemia positiva precedió a la febre en 3,5 días, a los hallazgos en la radiografía simple de tórax en 8 días, a la TAC torácica en 6 días y a los resultados del primer cultivo de secreciones respiratorias en 9 días37. Para obtener estos resultados, las muestras de sangre deben tomarse al menos 2 veces por semana38. El GM también se puede detectar en el BAL, orina o líquido céfalo raquídeo3.
En pacientes no neutropénicos es más difícil de valorar. No está bien establecido el valor de una determinación puntual; y parece difícil su medición repetida en pacientes no neutropénicos. En pacientes no neutropénicos los resultados son contradictorios. Unos autores defenden su utilidad, con una sensibilidad de 88% y especificidad de 87%39; y por el contrario, otros destacan los falsos positivos relacionados con la colonización fúngica en el lavado broncoalveolar de los pacientes no inmunodeprimidos con infiltrados pulmonares40.
Globalmente el GM tiene una sensibilidad de 71% y una especificidad de 89%, con un valor predictivo positivo entre 25% y 62%, y un valor predictivo negativo entre 92% y 98%, aunque con gran variabilidad entre los diferentes estudios41,42. Estas discrepancias se deben, entre otras causas, al número de tests realizados por semana, la definición utilizada de API y el punto de corte elegido37,41,42.
Una modificación en el proceso de las muestras de suero permite un incremento significativo de la sensibilidad del test de GM, además de acortar los tiempos de diagnóstico, aunque con una discreta disminución en la especificidad43.
El GM también se ha aplicado en pacientes con EPOC gravemente enfermos y sospecha de API. En un estudio con 25 pacientes, 12 fueron positivos (40%). Sin embargo, no se pueden extraer conclusiones definitivas debido a la pequeña muestra, el diseño retrospectivo del estudio y la ausencia de investigación sobre la existencia de factores confusores9. Una única determinación de GM podría ser útil para el diagnóstico de la API en pacientes no hematológicos44.
Un incremento en la antigenemia sobre un valor basal puede discriminar mejor que un simple valor por encima del normal. La elevación de la antigenemia durante la primera semana de observación estaba asociado con enfermedad progresiva, con una sensibilidad de 44%, una especificidad de 87%, y un valor predictivo positivo de 94%44. Un aumento en la antigenemia también podría ser indicativo de fallo en el tratamiento y, por tanto, nos permitiría anticipar la decisión de modificar el tratamiento45.
El test del GM tiene varias limitaciones. Solamente un tercio de los pacientes tenían una respuesta antigénica positiva antes de que el diagnóstico de API se hiciera por TC. Tampoco se ha demostrado reducción de la mortalidad con la utilización de esta prueba. Se han descrito falsos positivos en pacientes que estaban recibiendo tratamiento con piperacilina/tazobactan o amoxicilina/clavulánico; así como reacciones cruzadas con otros hongos, bacterias, ciclofosfamida y comidas (vegetales enlatados, pasta, arroz). Por último, se desconoce si los resultados obtenidos en enfermedades hematológicas malignas pueden extrapolarse a pacientes con otras enfermedades como la EPOC2,7,33,38,46,47.
Otras exploraciones de laboratorio, como la reacción en cadena de la polimerasa (PCR) o la concentración plasmática de β-D-glucano están en desarrollo. Resultados preliminares sugieren que la PCR tiene una buena sensibilidad y especificidad48. Sin embargo, no hay métodos estandarizados y validados, las definiciones de API varían en los distintos estudios y hay que ser precavidos porque productos del plasma podrían inhibir los test de PCR49. La determinación de la concentración plasmática de β-D-glucano, un componente de la pared celular del hongo, no parece superior a los test de PCR50.
Por otra parte, la producción de anticuerpos traduce la respuesta de la inmunidad humoral.
Constituyen un criterio diagnóstico en otras formas de enfermedad por Aspergillus, aunque su papel no está clarificado en la API7.
Radiología
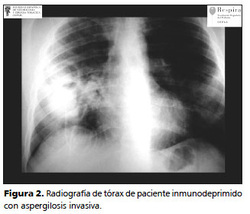
La radiografía de tórax puede ser normal en los estadios iniciales de la API. Se han descrito múltiples signos radiológicos asociados con API, tales como consolidación, nódulos, el signo del halo o el signo del aire creciente. Lo más frecuente es la presentación de consolidación pulmonar, que presentan alrededor de 60% de pacientes3,11.
En un contexto clínico compatible, la presencia de una o varias opacidades nodulares debe hacernos sospechar API (Figura 2).
Radiología
La radiografía de tórax puede ser normal en los estadios iniciales de la API. Se han descrito múltiples signos radiológicos asociados con API, tales como consolidación, nódulos, el signo del halo o el signo del aire creciente. Lo más frecuente es la presentación de consolidación pulmonar, que presentan alrededor de 60% de pacientes3,11.
En un contexto clínico compatible, la presencia de una o varias opacidades nodulares debe hacernos sospechar API (Figura 2).
La radiografía de tórax puede ser normal en los estadios iniciales de la API. Se han descrito múltiples signos radiológicos asociados con API, tales como consolidación, nódulos, el signo del halo o el signo del aire creciente. Lo más frecuente es la presentación de consolidación pulmonar, que presentan alrededor de 60% de pacientes3,11.
En un contexto clínico compatible, la presencia de una o varias opacidades nodulares debe hacernos sospechar API (Figura 2).
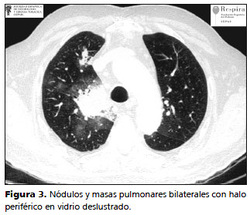
El signo del aire creciente es el resultado de tejido pulmonar infartado delimitado por un espacio lleno de aire52.
El signo del halo o el signo del aire creciente, aunque poco frecuentes, son casi patognomónicos de API en pacientes hematológicos; aunque parece que se observan con menos frecuencia en pacientes con EPOC y trasplantados de órganos sólidos donde consolidaciones inespecíficas son vistas con más frecuencia que los hallazgos específicos mencionados4,11,53.
Otra característica del signo del halo es que se hace menos frecuente con la evolución de la enfermedad. Así, se puede ver en 68% de pacientes a los 3 días de evolución, pero sólo en 22% en el séptimo día4,11.
La tomografía computarizada (TAC) parece especialmente importante en el diagnóstico de esta enfermedad. Se ha demostrado que permite anticipar la sospecha diagnóstica de API 4,7 días comparado con la radiografía simple de tórax; o 11,5 días si se compara con el B-D-glucano54. Incluso, en pacientes inmunodeprimidos, algunos estudios han hallado que el diagnóstico se puede establecer antes con TAC que con GM, aunque carecemos de datos comparativos en pacientes con EPOC, donde la reactividad podría ser distinta38.
La supervivencia puede mejorar cuando se realiza una TC torácica al inicio de la enfermedad porque es bastante más sensible para detectar tempranamente lesiones, que la radiografía de tórax55. Además, la TAC puede ser útil en el diagnóstico diferencial, donde se incluyen otras infecciones o procesos no infecciosos como linfomas, neoplasias o tromboembolismo pulmonar56.
El signo del halo o el signo del aire creciente, aunque poco frecuentes, son casi patognomónicos de API en pacientes hematológicos; aunque parece que se observan con menos frecuencia en pacientes con EPOC y trasplantados de órganos sólidos donde consolidaciones inespecíficas son vistas con más frecuencia que los hallazgos específicos mencionados4,11,53.
Otra característica del signo del halo es que se hace menos frecuente con la evolución de la enfermedad. Así, se puede ver en 68% de pacientes a los 3 días de evolución, pero sólo en 22% en el séptimo día4,11.
La tomografía computarizada (TAC) parece especialmente importante en el diagnóstico de esta enfermedad. Se ha demostrado que permite anticipar la sospecha diagnóstica de API 4,7 días comparado con la radiografía simple de tórax; o 11,5 días si se compara con el B-D-glucano54. Incluso, en pacientes inmunodeprimidos, algunos estudios han hallado que el diagnóstico se puede establecer antes con TAC que con GM, aunque carecemos de datos comparativos en pacientes con EPOC, donde la reactividad podría ser distinta38.
La supervivencia puede mejorar cuando se realiza una TC torácica al inicio de la enfermedad porque es bastante más sensible para detectar tempranamente lesiones, que la radiografía de tórax55. Además, la TAC puede ser útil en el diagnóstico diferencial, donde se incluyen otras infecciones o procesos no infecciosos como linfomas, neoplasias o tromboembolismo pulmonar56.
Biopsia
Como se ha dicho, solamente la histología puede confirmar la API junto a la presencia de otros criterios microbiológicos2 (Tabla 1). Las muestras de tejido pueden obtenerse mediante broncosco-pia, biopsia percutánea o biopsia pulmonar abierta. Cualquiera de estas técnicas, dada la gravedad basal del paciente con EPOC y sospecha de API, plantean dificultades para su realización4.
Durante la fibrobroncoscopia, pueden estar presentes algunas lesiones en la mucosa que se pueden biopsiar. La rentabilidad de estas biop-sias fue de 47% en pacientes con API probable o probada57,58.
La biopsia transbronquial tiene una sensibilidad en torno 25%36,57, pero es altamente específica, como parece demostrarse en un trabajo reciente, donde se demostraron Aspergillus invadiendo el parénquima pulmonar en todos los casos en que fue realizada, aunque los resultados deben ser tomados con cautela, ya que sólo se había realizado esta técnica en 5 pacientes3.
El tejido pulmonar puede ser obtenido también por biopsia percutánea con una rentabilidad de aproximadamente 50%, si bien el resultado negativo no excluye el diagnóstico32. Esta técnica está especialmente indicada en lesiones periféricas, aunque el riesgo de neumotórax es importante en pacientes con EPOC59.
Además, la resección pulmonar puede ser también una herramienta terapéutica14.
Conclusiones
Aunque la colonización por Aspergillus spp es frecuente en los pacientes con EPOC, la API puede afectar a estos enfermos por lo que es muy importante establecer el diagnóstico lo antes posible para conseguir el mayor éxito terapéutico.
Debe sospecharse API en el paciente EPOC con una infección respiratoria resistente a los antibióticos y aspecto radiológico sugerente. En estos casos debe realizarse estudio de secreciones respiratorias, de los antígenos deAspergillus y una TAC torácica. Este último estudio nos permitirá observar pequeños cambios en el parénquima pulmonar, anticipando la sospecha diagnóstica.
No hay suficientes datos para apoyar el uso de test serológicos (detección de galactomanano y anticuerpos) para establecer el diagnóstico, aunque los datos disponibles parecen prometedores.
Si el estado del paciente es grave, debería de iniciarse el tratamiento de forma empírica para proporcionarle mayores posibilidades de curación y, posteriormente, deben de realizarse los procedimientos diagnósticos necesarios para confirmar la sospecha clínica de API.
Los criterios diagnósticos establecidos para pacientes neutropénicos no son aplicables de forma definitiva en pacientes con otras características.
El diagnóstico definitivo requiere la confirmación histológica junto a la presencia de otros criterios microbiológicos o serológicos.
A los pacientes que reciban tratamiento crónico con corticoides, se les debería de proporcionar información acerca de cómo prevenir el contacto con fuentes medioambientales de Aspergillus spp.
Se necesitan llevar a cabo más trabajos para mejorar el conocimiento de la infección por As-pergillus en pacientes con EPOC y poder disminuir así la mortalidad de esta devastadora enfermedad
Como se ha dicho, solamente la histología puede confirmar la API junto a la presencia de otros criterios microbiológicos2 (Tabla 1). Las muestras de tejido pueden obtenerse mediante broncosco-pia, biopsia percutánea o biopsia pulmonar abierta. Cualquiera de estas técnicas, dada la gravedad basal del paciente con EPOC y sospecha de API, plantean dificultades para su realización4.
Durante la fibrobroncoscopia, pueden estar presentes algunas lesiones en la mucosa que se pueden biopsiar. La rentabilidad de estas biop-sias fue de 47% en pacientes con API probable o probada57,58.
La biopsia transbronquial tiene una sensibilidad en torno 25%36,57, pero es altamente específica, como parece demostrarse en un trabajo reciente, donde se demostraron Aspergillus invadiendo el parénquima pulmonar en todos los casos en que fue realizada, aunque los resultados deben ser tomados con cautela, ya que sólo se había realizado esta técnica en 5 pacientes3.
El tejido pulmonar puede ser obtenido también por biopsia percutánea con una rentabilidad de aproximadamente 50%, si bien el resultado negativo no excluye el diagnóstico32. Esta técnica está especialmente indicada en lesiones periféricas, aunque el riesgo de neumotórax es importante en pacientes con EPOC59.
Además, la resección pulmonar puede ser también una herramienta terapéutica14.
Conclusiones
Aunque la colonización por Aspergillus spp es frecuente en los pacientes con EPOC, la API puede afectar a estos enfermos por lo que es muy importante establecer el diagnóstico lo antes posible para conseguir el mayor éxito terapéutico.
Debe sospecharse API en el paciente EPOC con una infección respiratoria resistente a los antibióticos y aspecto radiológico sugerente. En estos casos debe realizarse estudio de secreciones respiratorias, de los antígenos deAspergillus y una TAC torácica. Este último estudio nos permitirá observar pequeños cambios en el parénquima pulmonar, anticipando la sospecha diagnóstica.
No hay suficientes datos para apoyar el uso de test serológicos (detección de galactomanano y anticuerpos) para establecer el diagnóstico, aunque los datos disponibles parecen prometedores.
Si el estado del paciente es grave, debería de iniciarse el tratamiento de forma empírica para proporcionarle mayores posibilidades de curación y, posteriormente, deben de realizarse los procedimientos diagnósticos necesarios para confirmar la sospecha clínica de API.
Los criterios diagnósticos establecidos para pacientes neutropénicos no son aplicables de forma definitiva en pacientes con otras características.
El diagnóstico definitivo requiere la confirmación histológica junto a la presencia de otros criterios microbiológicos o serológicos.
A los pacientes que reciban tratamiento crónico con corticoides, se les debería de proporcionar información acerca de cómo prevenir el contacto con fuentes medioambientales de Aspergillus spp.
Se necesitan llevar a cabo más trabajos para mejorar el conocimiento de la infección por As-pergillus en pacientes con EPOC y poder disminuir así la mortalidad de esta devastadora enfermedad