PARACOCCIDIOMICOSIS EN CASOS DE TBC ASOCIADA A VIH/VHC
Introducción
Paracoccidiomicosis (PCM) es la micosis sistémica de mayor prevalencia en América latina1. En el Perú se presenta sólo en las regiones de ceja de selva y selva baja amazónica, debido a que estas zonas de clima tropical reúnen las condiciones ecológicas apropiadas para la supervivencia de Paracoccidioides brasiliensis. Esta micosis no existe en forma autóctona ni en la costa ni en la región andina. Desde 1937 hasta 1971 fueron diagnosticados en el Perú, 147 casos2.
El síndrome de inmunodeficiencia adquirida (SIDA) se caracteriza por el desarrollo de varias infecciones oportunistas que incluyen micosis superficiales y profundas. Candida albicans, Criptococcus neoformans eHistoplasma capsulatum son las micosis oportunistas más frecuentemente reportadas3.
La co-infección PCM/SIDA es raramente reportada. Hasta el año 2005 fueron publicados 84 casos con dicha asociación4. La tuberculosis (TBC) es una de las infecciones oportunistas (10) prevalentes en la población infectada con VIH en el Perú5 6; asociada a PCM y SIDA se han reportado casos solamente en Brasil7. No se ha encontrado reporte similar alguno al caso presentado, en la literatura revisada.
Caso Clínico
Varón de 54 años de edad, bisexual, enfermero retirado. Natural del Departamento de Huánuco. Historia de viajes frecuentes a su lugar de nacimiento. Pasatiempo: espeleología. No usuario de drogas. Diagnóstico de infección por VIH en el año 2000. En agosto del 2006 consultó por fiebre y diarrea. Sin medicación profiláctica para IO. El examen físico reveló microadenopatías cervicales e inguinales. IMC: 23 kg/m2. Exámenes de laboratorio: Reacción inflamatoria en heces: Leucocitos > 100/campo, PMN (99%), moco (+++), sangre (-). Coprocultivo (-). Hemograma: Leucocitos: 10.300/mm3, Hb: 9,3 g/dL, plaquetas: 823.000/mm3. Pruebas hepáticas: Fosfatasa alcalina (FA): 458 U/L, gamma-glutamiltrasferasa (GGT): 158 U/L, transaminasa glutámico oxalacética (TGO): 62 U/L, albuminemia: 2 g%. En junio 2006 el recuento de células CD4 fue de 108 células/ mm3 y la carga viral VIH de 1.064 543 copias/ml.
Tras la terapia inicial y remisión de la diarrea, el paciente evolucionó con alzas febriles intermitentes, dolor abdominal tipo cólico difuso, de moderada intensidad. Se amplió el estudio: aspirado y cultivo de médula ósea (-). BAAR en esputo (x3): negativo. Hemocultivos: negativos. TAC abdominal: hepatomegalia y ausencia de cálculos. Anticuerpos para VHC: reactivo. Carga viral VHC: 1.166 Ul/ml, (3.147 copias/ml).
En los exámenes de control se observó un mayor aumento de GGT (397 U/L) y FA: (1.476 U/L). Ante la sospecha de una micosis profunda diseminada se inició terapia con anfotericina (0,7 mg/kg/día); la cual recibió en días alternos hasta la dosis acumulada de 600 mg, siendo suspendida por elevación de la creatininemia a 1,7 mg/dL. La fiebre remitió al décimo día de tratamiento, continuándose con fluconazol ev. Resultado de cultivo de BAAR en esputo: crecimiento de una colonia. Se realizó resembrado.
Durante la fase de mantenimiento con fluconazol reapareció la fiebre, por lo que se realizó una punción lumbar obteniéndose los siguientes resultados: glucosa: 33 mg/dl, ADA: 5,5 U/1, proteínas: 47,4 mg/dl, tinta china (-). Se envió muestra de LCR para cultivo de bacilo de Koch.
El paciente evolucionó con la aparición de nodulos subcutáneos en la pared abdominal se realizó biopsia hepática, cuyo resultado fue hepatitis granulomatosa. BAAR (-).
Paracoccidiomicosis (PCM) es la micosis sistémica de mayor prevalencia en América latina1. En el Perú se presenta sólo en las regiones de ceja de selva y selva baja amazónica, debido a que estas zonas de clima tropical reúnen las condiciones ecológicas apropiadas para la supervivencia de Paracoccidioides brasiliensis. Esta micosis no existe en forma autóctona ni en la costa ni en la región andina. Desde 1937 hasta 1971 fueron diagnosticados en el Perú, 147 casos2.
El síndrome de inmunodeficiencia adquirida (SIDA) se caracteriza por el desarrollo de varias infecciones oportunistas que incluyen micosis superficiales y profundas. Candida albicans, Criptococcus neoformans eHistoplasma capsulatum son las micosis oportunistas más frecuentemente reportadas3.
La co-infección PCM/SIDA es raramente reportada. Hasta el año 2005 fueron publicados 84 casos con dicha asociación4. La tuberculosis (TBC) es una de las infecciones oportunistas (10) prevalentes en la población infectada con VIH en el Perú5 6; asociada a PCM y SIDA se han reportado casos solamente en Brasil7. No se ha encontrado reporte similar alguno al caso presentado, en la literatura revisada.
Caso Clínico
Varón de 54 años de edad, bisexual, enfermero retirado. Natural del Departamento de Huánuco. Historia de viajes frecuentes a su lugar de nacimiento. Pasatiempo: espeleología. No usuario de drogas. Diagnóstico de infección por VIH en el año 2000. En agosto del 2006 consultó por fiebre y diarrea. Sin medicación profiláctica para IO. El examen físico reveló microadenopatías cervicales e inguinales. IMC: 23 kg/m2. Exámenes de laboratorio: Reacción inflamatoria en heces: Leucocitos > 100/campo, PMN (99%), moco (+++), sangre (-). Coprocultivo (-). Hemograma: Leucocitos: 10.300/mm3, Hb: 9,3 g/dL, plaquetas: 823.000/mm3. Pruebas hepáticas: Fosfatasa alcalina (FA): 458 U/L, gamma-glutamiltrasferasa (GGT): 158 U/L, transaminasa glutámico oxalacética (TGO): 62 U/L, albuminemia: 2 g%. En junio 2006 el recuento de células CD4 fue de 108 células/ mm3 y la carga viral VIH de 1.064 543 copias/ml.
Tras la terapia inicial y remisión de la diarrea, el paciente evolucionó con alzas febriles intermitentes, dolor abdominal tipo cólico difuso, de moderada intensidad. Se amplió el estudio: aspirado y cultivo de médula ósea (-). BAAR en esputo (x3): negativo. Hemocultivos: negativos. TAC abdominal: hepatomegalia y ausencia de cálculos. Anticuerpos para VHC: reactivo. Carga viral VHC: 1.166 Ul/ml, (3.147 copias/ml).
En los exámenes de control se observó un mayor aumento de GGT (397 U/L) y FA: (1.476 U/L). Ante la sospecha de una micosis profunda diseminada se inició terapia con anfotericina (0,7 mg/kg/día); la cual recibió en días alternos hasta la dosis acumulada de 600 mg, siendo suspendida por elevación de la creatininemia a 1,7 mg/dL. La fiebre remitió al décimo día de tratamiento, continuándose con fluconazol ev. Resultado de cultivo de BAAR en esputo: crecimiento de una colonia. Se realizó resembrado.
Durante la fase de mantenimiento con fluconazol reapareció la fiebre, por lo que se realizó una punción lumbar obteniéndose los siguientes resultados: glucosa: 33 mg/dl, ADA: 5,5 U/1, proteínas: 47,4 mg/dl, tinta china (-). Se envió muestra de LCR para cultivo de bacilo de Koch.
El paciente evolucionó con la aparición de nodulos subcutáneos en la pared abdominal se realizó biopsia hepática, cuyo resultado fue hepatitis granulomatosa. BAAR (-).
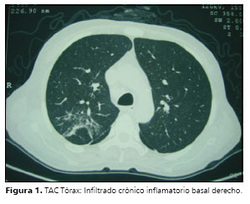
TAC tórax: infiltrado basal derecho (Figura 1). Ante la probabilidad de una TBC diseminada se decidió empezar tratamiento específico, esquema I del Programa Nacional Control de Tuberculosis (isoniacida + rifampicina + pirazinamida + etambutol) presentando el caso, al séptimo día de tratamiento, reacción adversa a fármacos anti-TBC (RAFA) hepático y aumento de la amilasemia. Fue suspendida toda la medicación.
El paciente evolucionó con tos persistente y disnea por lo que recibió tratamiento para neumonía intrahospitalaria(ciprofloxacina + ceftazidima) observándose una mejoría clínica pero continuó con tos leve.
Fue reiniciado tratamiento anti-TBC con el siguiente esquema: estreptomicina 600 mg/día + etambutol 30 mg/ kg-peso/día, continuando con ciprofloxacina 400 mg/día ev dos veces por día. Resultado de cultivo de micobacte-rias en el LCR: Mycobacterium sp.
El paciente evolucionó con tos persistente y disnea por lo que recibió tratamiento para neumonía intrahospitalaria(ciprofloxacina + ceftazidima) observándose una mejoría clínica pero continuó con tos leve.
Fue reiniciado tratamiento anti-TBC con el siguiente esquema: estreptomicina 600 mg/día + etambutol 30 mg/ kg-peso/día, continuando con ciprofloxacina 400 mg/día ev dos veces por día. Resultado de cultivo de micobacte-rias en el LCR: Mycobacterium sp.
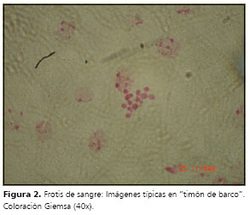
Una muestra sanguínea del paciente fue enviada al Instituto de Medicina Tropical de la Universidad Nacional Mayor de San Marcos, encontrándose positivo a P. bra-siliensis en el frotis, (Figura 2) con cultivo negativo. La revisión de la biopsia hepática realizada anteriormente, confirmó el compromiso hepático micótico (Figura 3) iniciándose tratamiento con itraconazol 100 mg dos veces al día.
En diciembre 2009, el recuento de CD4 descendió a 19 células/mm3 y la carga viral para VIH fue de 457.500 copias/ml.
El paciente continuó con tos leve y dolor abdominal esporádico asociado a aumento de amilasemia. Se solicitó serología para citomegaloviras (CMV): IgG 19,1 Ul/ml, IgM 1,5 Ul/ml (Reactivo > 1,1 Ul/ml).
En diciembre 2009, el recuento de CD4 descendió a 19 células/mm3 y la carga viral para VIH fue de 457.500 copias/ml.
El paciente continuó con tos leve y dolor abdominal esporádico asociado a aumento de amilasemia. Se solicitó serología para citomegaloviras (CMV): IgG 19,1 Ul/ml, IgM 1,5 Ul/ml (Reactivo > 1,1 Ul/ml).
Discusión
Paracoccidioidomicosis (PCM) es una infección producida por el hongo P. brasiliensis, que se restringe a Latinoamérica8. En el Perú existen pocos trabajos realizados respecto a esta micosis. Burstein2 realizó una revisión de 111 casos desde el año 1937, reportando que los casos fueron procedentes con mayor frecuencia de las zonas selváticas de los Departamentos de Junín y Huanuco. Encontró además que las edades entre 31 y 60 años de edad fue el grupo más afectado.
Paracoccidioidomicosis tiene varios factores de riesgo asociados a su adquisición y desarrollo: procedencia de zona endémica, sexo masculino y, en pacientes con infección por VIH; la falta de profilaxis con cotrimoxazol''; todos ellos estaban presentes en este caso.
La prevalencia estimada de PCM entre personas infectadas con el VIH en algunos estados de Brasil es relativamente baja cuando se compara con otras micosis tales como histoplasmosis y criptococosis10. Hasta marzo del 2003 en dicho país fueron publicados 104 casos de PCM en pacientes con VIH/SIDA, lo cual contrasta con los 2.500 casos de SIDAe histoplasmosis11. Generalmente los pacientes co-infectados PCM/VIH, tienen un recuento de linfocitos T CD4 inferior a 200 células/mm3 12. La actual baja incidencia de PCM en pacientes con infección por VIH puede atribuirse al uso extendido de TARGA y al uso de cotrimoxazol como profilaxis, ya que ésta es un fármaco efectivo contra PCM13.
En inmunocomprometidos con PCM, la reactivación lleva hacia una enfermedad mixta diseminada3. En el caso presentado, el diagnóstico etiológico se basó en el hallazgo de levaduras de P. brasiliensis en sangre más un compromiso hepático granulomatoso micótico. Se considera al examen directo micológico como el estándar de oro para el diagnóstico de PCM14; la confirmación de un caso probable puede ser realizada a través de este modo15aunque su detección en sangre a través del frotis no es lo habitual16.
Es probable que el cultivo negativo para PCM que obtuvimos haya sido por el reinicio de la profilaxis con cotrimoxazol en los días previos.
El caso presentó una recaída con el uso de fluconazol debido a que el anti-fungico de elección en PCM es itraconazol17.
En el Perú, los pacientes infectados con el VIH están en riesgo de contraer y morir por M. tuberculosis, siendo la TBC multiresistente (MR) un problema emergente. La TBC-MR en el Perú se asocia a tratamiento inadecuado, pobre adherencia al tratamiento e infección por VIH18'19. En el caso presentado además de la infección por VIH se agregó como factor de riesgo, una estancia hospitalaria prolongada.
El crecimiento de una colonia en el cultivo de BK en esputo, como ocurrió en nuestro paciente, es indicativo de TBC pulmonar, dado que el crecimiento deM tuberculosis no se da por contaminación. La baciloscopia en esputo fue negativa, lo cual puede ser explicado por su condición de inmunosuprimido siendo común que en pacientes con infección por VIH se manifieste un cuadro clínico atípico y sea común la diseminación extrapulmonar, así como los eventos adversos relacionados al tratamiento20.
Cerca de un tercio de los pacientes infectados con VIH tienen hepatitis C crónica, llegando esta tasa hasta 75% en usuarios de drogas ev21. En la actualidad existe una mayor evidencia de transmisión vía sexual del VHC22-23. El caso presentado tuvo antecedentes de exposición sexual (bisexual) y posiblemente parenteral (enfermero que había trabajado en un servicio quirúrgico).
Los pacientes co-infectados por VIH y VHC tienen una rápida progresión de la hepatitis, con aumento de la carga viral y daño hepático grave lo cual aumenta el riesgo de muerte por enfermedad hepática24. Sin embargo, en el caso descrito la disfunción hepática fue multifactorial. (Inicialmente fue tóxica por isoiacida y/o rifampicina; finalmente por nevirapina y fármaco antipsicótico).
La recomendación en pacientes co-infectados con VIH/ VHC es empezar TARGA25, aunque el VHC es a su vez, un fuerte predictor para el desarrollo de hepatotoxicidad por TARGA2627. Se ha reportado que la enfermedad crónica hepática más frecuente en pacientes co-infectados por PCM y VIH es causada por el VHC28.
Durante la evolución, el paciente presentó elevación de la amilasemia concomitante al inicio de tratamiento anti TBC; sin embargo, al suspenderse dicha terapia permanecieron elevados los controles de amilasemia y el dolor abdominal, lo cual sugirió otra etiología.
El paciente tuvo serología de reactivación para CMV concomitante a la caída de células CD4 a < 50 células/ mm3. Además se diagnóstico retinitis por CMV asintomá-tica por lo que se consideró al CMV como etiología del dolor abdominal y del aumento de la amilasemia. El CMV es el microorganismo que más frecuentemente afecta el páncreas en pacientes infectados por VIH, siendo el compromiso a menudo silente y de reconocimiento difícil, por lo que no es sospechado; su diagnóstico generalmente es post mortem29~31. En nuestro caso no se pudo confirmar el compromiso pancreático por CMV dado que no se realizó necropsia.
Paracoccidioidomicosis (PCM) es una infección producida por el hongo P. brasiliensis, que se restringe a Latinoamérica8. En el Perú existen pocos trabajos realizados respecto a esta micosis. Burstein2 realizó una revisión de 111 casos desde el año 1937, reportando que los casos fueron procedentes con mayor frecuencia de las zonas selváticas de los Departamentos de Junín y Huanuco. Encontró además que las edades entre 31 y 60 años de edad fue el grupo más afectado.
Paracoccidioidomicosis tiene varios factores de riesgo asociados a su adquisición y desarrollo: procedencia de zona endémica, sexo masculino y, en pacientes con infección por VIH; la falta de profilaxis con cotrimoxazol''; todos ellos estaban presentes en este caso.
La prevalencia estimada de PCM entre personas infectadas con el VIH en algunos estados de Brasil es relativamente baja cuando se compara con otras micosis tales como histoplasmosis y criptococosis10. Hasta marzo del 2003 en dicho país fueron publicados 104 casos de PCM en pacientes con VIH/SIDA, lo cual contrasta con los 2.500 casos de SIDAe histoplasmosis11. Generalmente los pacientes co-infectados PCM/VIH, tienen un recuento de linfocitos T CD4 inferior a 200 células/mm3 12. La actual baja incidencia de PCM en pacientes con infección por VIH puede atribuirse al uso extendido de TARGA y al uso de cotrimoxazol como profilaxis, ya que ésta es un fármaco efectivo contra PCM13.
En inmunocomprometidos con PCM, la reactivación lleva hacia una enfermedad mixta diseminada3. En el caso presentado, el diagnóstico etiológico se basó en el hallazgo de levaduras de P. brasiliensis en sangre más un compromiso hepático granulomatoso micótico. Se considera al examen directo micológico como el estándar de oro para el diagnóstico de PCM14; la confirmación de un caso probable puede ser realizada a través de este modo15aunque su detección en sangre a través del frotis no es lo habitual16.
Es probable que el cultivo negativo para PCM que obtuvimos haya sido por el reinicio de la profilaxis con cotrimoxazol en los días previos.
El caso presentó una recaída con el uso de fluconazol debido a que el anti-fungico de elección en PCM es itraconazol17.
En el Perú, los pacientes infectados con el VIH están en riesgo de contraer y morir por M. tuberculosis, siendo la TBC multiresistente (MR) un problema emergente. La TBC-MR en el Perú se asocia a tratamiento inadecuado, pobre adherencia al tratamiento e infección por VIH18'19. En el caso presentado además de la infección por VIH se agregó como factor de riesgo, una estancia hospitalaria prolongada.
El crecimiento de una colonia en el cultivo de BK en esputo, como ocurrió en nuestro paciente, es indicativo de TBC pulmonar, dado que el crecimiento deM tuberculosis no se da por contaminación. La baciloscopia en esputo fue negativa, lo cual puede ser explicado por su condición de inmunosuprimido siendo común que en pacientes con infección por VIH se manifieste un cuadro clínico atípico y sea común la diseminación extrapulmonar, así como los eventos adversos relacionados al tratamiento20.
Cerca de un tercio de los pacientes infectados con VIH tienen hepatitis C crónica, llegando esta tasa hasta 75% en usuarios de drogas ev21. En la actualidad existe una mayor evidencia de transmisión vía sexual del VHC22-23. El caso presentado tuvo antecedentes de exposición sexual (bisexual) y posiblemente parenteral (enfermero que había trabajado en un servicio quirúrgico).
Los pacientes co-infectados por VIH y VHC tienen una rápida progresión de la hepatitis, con aumento de la carga viral y daño hepático grave lo cual aumenta el riesgo de muerte por enfermedad hepática24. Sin embargo, en el caso descrito la disfunción hepática fue multifactorial. (Inicialmente fue tóxica por isoiacida y/o rifampicina; finalmente por nevirapina y fármaco antipsicótico).
La recomendación en pacientes co-infectados con VIH/ VHC es empezar TARGA25, aunque el VHC es a su vez, un fuerte predictor para el desarrollo de hepatotoxicidad por TARGA2627. Se ha reportado que la enfermedad crónica hepática más frecuente en pacientes co-infectados por PCM y VIH es causada por el VHC28.
Durante la evolución, el paciente presentó elevación de la amilasemia concomitante al inicio de tratamiento anti TBC; sin embargo, al suspenderse dicha terapia permanecieron elevados los controles de amilasemia y el dolor abdominal, lo cual sugirió otra etiología.
El paciente tuvo serología de reactivación para CMV concomitante a la caída de células CD4 a < 50 células/ mm3. Además se diagnóstico retinitis por CMV asintomá-tica por lo que se consideró al CMV como etiología del dolor abdominal y del aumento de la amilasemia. El CMV es el microorganismo que más frecuentemente afecta el páncreas en pacientes infectados por VIH, siendo el compromiso a menudo silente y de reconocimiento difícil, por lo que no es sospechado; su diagnóstico generalmente es post mortem29~31. En nuestro caso no se pudo confirmar el compromiso pancreático por CMV dado que no se realizó necropsia.
